a. Keisomeran karena atom karbon asimetrik, keisomeran optik
Sebelum ada teori valensi, kimiawan/fisiologis Perancis Louis Pasteur (1822-1895) telah mengenali pengaruh struktur molekul individual pada sifat gabungan molekul. Ia berhasil memisahkan asam rasemat tartarat (sebenarnya garam natrium amonium) menjadi (+) dan (-) berdasarkan arah muka hemihedral kristalnya (1848).
Kedua senyawa memiliki sifat fisika (misalnya titik leleh) dan kimia yang sama, tetapi ada perbedaan dalam sifat optik dalam larutan masing-masing senyawa. Keduanya memutar bidang polarisasi cahaya, dengan kata lain mempunyai keaktifan optik. Rotasi jenis kedua senyawa, yang mengkur kekuatan rotasi kedua senyawa, memiliki nilai absolut yang sama, namun tandanya berlawanan. Karena molekul berada bebas dalam larutan, perbedaan ini tidak dapat dijelaskan karena perbedaan struktur kristal. Sayangnya waktu itu, walaupun teori atom sudah ada, teori valensi belum ada. Dengan kondisi seperti ini Pasteur tidak dapat menjelaskan penemuannya.
Di tahun 1860-an, kimiawan Jerman Johannes Adolf Wislicenus (1835-1902) menemukan bahwa dua jenis asam laktat yang diketahui itu keduanya adalah asam α-hidroksipropanoat CH3CH(OH)COOH, bukan asam β- hidroksipropanoat HOCH2CH2COOH. Ia lebih lanjut menyarankan bahwa konsep baru untuk stereoisomer harus dibuat untuk menjelaskna fenomena ini. Konse baru ini menyatakan bahwa kedua senyawa yang memiliki rumus struktur yang sama dalam dua dimensu dapat menjadi stereoisomer bila susunan atom-atomnya di ruang berbeda.
Di tahun 1874, van’t Hoff dan Le Bel secara independen mengusulkan teori atom karbon tetrahedral. Menurut teori ini, kedua asam laktat yang dapat digambarkan di Gambar 4.4. Salah satu asam laktat adalah bayangan cermin asam laktat satunya. Dengan kata lain, hubungan kedua senyawa seperti hubungan tangan kanan dan tangan kiri, dan oleh karena itu disebut dengan antipoda atau enantiomer. Berkat teori van’t Hoff dan Le Bel, bidang kimia baru, stereokimia, berkembang dengan cepat.
(+)-asam laktat (-)-lactic acid
Gambar 4.4 Stereoisomer asam laktat.
Kedua isomer atau antipoda, berhubungan layaknya tangan kanan dan kiri
Pada atom karbon pusat di asam laktat, empat atom atau gigus yang berbeda terikat. Atom karbon semacam ini disebut dengan atom karbon asimetrik. Umumnya, jumlah stereoisomer akan sebanyak 2n, n adalah jumlah atom karbon asimetrik. Asam tartarat memiliki dua atom karbon asimetrik. Namun, karena keberadaan simetri molekul, jumlah stereoisomernya kurang dari 2n, dan lagi salah satu stereoisomer secara optik tidak aktif (Gambar 4.5). Semua fenomena ini dapat secara konsisten dijelaskan dengan teori atom karbon tetrahedral.
(+)-asam tartarat (-)-asam tartarat meso-asam tartarat
Gambar 4.5 Stereoisomer asam tartarat(+)-asam tartarat dan (-)-asam tartarat membentuk pasangan enantiomer.
Namun karena adanya simetri, meso-asam tartarat secara optik tidak aktif.
b. Isomer geometri
Van’t Hoff menjelaskan keisomeran asam fumarat dan maleat karena batasan rotasi di ikatan ganda, suatu penjelasan yang berbeda dengan untuk keisomeran optik. Isomer jenis ini disebut dengan isomer geometri. Dalam bentuk trans subtituennya (dalam kasus asam fumarat dan maleat, gugus karboksil) terletak di sisi yang berbeda dari ikatan rangkap, sementara dalam isomer cis-nya subtituennya terletak di sisi yang sama.
Dari dua isomer yang diisoasi, van’t Hoff menamai isomer yang mudah melepaskan air menjadi anhidrida maleat isomer cis sebab dalam isomer cis kedua gugus karboksi dekat satu sama lain. Dengan pemanasan sampai 300 °C, asam fuarat berubah menjadi anhidrida maleat. Hal ini cukup logis karena prosesnya harus melibatkan isomerisasi cis-trans yang merupakan proses dengan galangan energi yang cukup tinggi (Gambar 4.6).
Karena beberapa pasangan isomer geometri telah diketahui, teori isomer geometri memberikan dukunagn yang baik bagi teori struktural van’t Hoff.
asam fumarat asam maleat anhidrida maleat
Gambar 4.6 Isomer geometri asam maleat (bentuk cis) mempunyai dua gugus karboksil yang dekat, dan mudah melepas air menjadi anhidrida (anhidrida maleat).
Dan pada kasus yang kedua akan ada isomer geometri.
Struktur benzen
Struktur benzen menjadi enigma beberapa tahun. Di tahun 1865, Kekulé mengusulkan struktur siklik planar dengan tiga ikatan tunggal dan tiga ikatan ganda yang terhubungkan secara bergantian. Strukturnya disebut dengan struktur Kekulé. Bukti struktur semacam ini datang dari jumlah isomer benzen tersubstitusi. Dengan struktur Kekulé, akan ada tiga isomer kresol, yakni, o, m- dan p-kresol (Gambar 4.7).
Struktur Kekulé tidak dapat menyelesaikan semua masalah yang berkaitan dengan struktur benzene. Bila benzene memiliki struktur seperti yang diusulkan Kekulé, akan ada dua isomer okresol, yang tidak diamati. Kekulé mempostulatkan bahwa ada kesetimbangan cepat, yang disebut dengan resonansi antara kedua struktur. Istilah resonansi kemudian digunakan dalam mekanika kuantum.
d. Struktur etana: analisis konformasional
Teori atom karbon tetrahedral dan struktur benzene memberikan fondasi teori struktur senyawa organik. Namun, van’t Hoff dan kimiawan lain mengenali bahwa masih ada masalah yang tersisa dan tidak dapat dijelaskan dengan teori karbon tetrahedral. Masalah itu adalah keisomeran yang disebabkan oleh adanya rotasi di sekitar ikatan tunggal.
Bila rotasi di sekitar ikatan C-C dalam 1,2-dikhloroetana CH2ClCH2Cl terbatas sebagaimana dalam kasus asam fumarat dan maleat, maka akan didapati banyak sekali isomer. Walaupun van’t Hoff awalnya menganggap adanya kemungkinan seperti itu, ia akhirnya menyimpulkan bahwa rotasinya bebas (rotasi bebas) karena tidak didapati isomer rotasional akibat batasan rotasi tersebut. Ia menambahkan bahwa struktur yang diamati adalah rata-rata dari semua struktur yang mungkin.
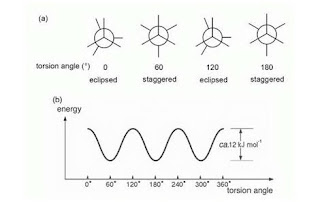
Di tahun 1930-an dibuktikan dengan teori dan percobaan bahwa rotasi di sekitar ikatan tunggal tidak sepenuhnya bebas. Dalam kasus etana, tolakan antara atom hidrogen yang terikat di atom karbon dekatnya akan membentuk halangan bagi rotasi bebas, dan besarnya tolakan akan bervariasi ketika rotasi tersebut berlangsung. Gambar 4.8(a) adalah proyeksi Newman etana, dan Gambar 4.8(b) adalah plot energi-sudut torsi.
Gambar 4.8 Analisis konformasional.
Dalam gambar (a) (proyeksi Newman), Anda dapat melihat molekul di arah ikatan C-C. Atom karbon depan dinyatakan dengan titik potong tiga garis pendek (masing-masing mewakili ikatan CH) sementara lingkaran mewakili arom karbon yang belakang. Keseluruhan gambar akan berkaitan dengan proyeksi molekul di dinding di belakangnya. Demi kesederhanaan atom hidrogennya tidak digambarkan (b) Bila sudut orsinya 0°, 120°, 240° dan 360°, bagian belakang molekul “berimpitan” eclipsed dengan bagian depan. Bila anda menggambarkan proyeksi Newman dengan tepat berimpit, anda sama sekali tidak dapat melihat bagian belakang. Secara konvensi, bagian belakang diputar sedikit agar dapat dilihat.
Bila sudut rotasi (sudut torsi) 0°, 60°, 120° dan 180°, energi molekul kalau tidak maksimum akan minimum. Struktur (konformasi) dengan sudut torsi 0° atau 120° disebut dengan bentuk eklips, dan konformasi dengan sudut torsi 60°atau 180° disebut bentuk staggered. Studi perubahan >struktur molekular yang diakibatkan oleh rotasi di sekitar ikatan tunggal disebut dengan analisis konformasional. Analisis ini telah berkembang sejak tahun 1950-an hingga kini.
Analisis konformasional butana CH3CH2CH2CH3 atas rotasi di sekitar ikatan C-C pusat, mengungkapkan bahwa ada dua bentuk staggered. Bentuk trans, dengan dua gugus metil terminal di sisi yang berlawanan, berenergi 0,7 kkal mol–1 lebih rendah (lebih stabil) daripada isomer gauche yang dua gugus metilnya berdekatan.
Hasil ini dapat diperluas ke senyawa-senyawa semacam pentana dan heksana yang memiliki lingkungan metilena tambahan, dan akhirnya pada poloetilena yang dibentuk oleh sejumlah besar metilen yang terikat. Dalam semua analisis ini, struktur trans, yakni struktur zig zag, adalah yang paling stabil. Namun, ini hanya benar dalam larutan. Untuk wujud padatnya faktor lain harus ikut diperhatikan.
hibridisasi atom karbon yang terlibat. Bila banyak konformasi dimungkinkan oleh adanya rotasi di sekitar ikatan tunggal, konformasi yang paling stabil akan dipilih.
Bila molekulnya memiliki sisi polar, faktor lain mungkin akan terlibat. Interaksi tarik menarik antara sisi positif dan negatif akan mengakibatkan struktur dengan halangan sterik terbesar lebih stabil. Dalam kasus asam salisilat, ikatan hidrogen antara gugus hidroksi dan karboksi akan membuat struktur yang lebih rapat lebih stabil
1. Perbedaan dalam sifat optik dalam larutan masing2 senyawa, ke duanya memutar bidang polarisasi cahaya disebut ?
Jawab : keaktifan optik
2. hubungan kedua senyawa seperti hubungan tangan kanan dan tangan kiri di sebut?
Jawab : antipoda atau enantiomer
3. atom karbon pusat di asam laktat, empat atom atau gigus yang berbeda terikat disebut ?
jawab : atom karbon asimetrik
4. keisomeran asam fumarat dan maleat karena batasan rotasi di ikatan ganda di sebut ?
jawab : isomergeometri
5. struktur siklir planar dengan tiga ikatan tunggal dan tiga ikatan ganda yang terhubungkan secara bergantian di sebut ?
jawab : struktur kekule.
 Bila suatu unsur memiliki lebih dari satu oksida, oksida dengan bilangan oksidasi lebih tinggi memiliki keasaman yang lebih besar daripada yang berbilangan oksidasi lebih rendah. Untuk belerang, SO2 (asam oksonya; H2SO3) adalah asam lemah tetapi SO3 (H2SO4) adalah asam kuat. Keasaman oksida khlorin meningkat dengan urutan sebagai yang ditunjukkan berikut ini.
Bila suatu unsur memiliki lebih dari satu oksida, oksida dengan bilangan oksidasi lebih tinggi memiliki keasaman yang lebih besar daripada yang berbilangan oksidasi lebih rendah. Untuk belerang, SO2 (asam oksonya; H2SO3) adalah asam lemah tetapi SO3 (H2SO4) adalah asam kuat. Keasaman oksida khlorin meningkat dengan urutan sebagai yang ditunjukkan berikut ini.